医药行业周报:再生元重磅抗炎药获FDA优先审评资格,用于治疗CRSwNP太平洋2024-05-20.pdf



摘要:报告摘要市场表现:2024年5月14日,医药板块涨跌幅+0.72%,跑赢沪深300指数0.93pct,涨跌幅居申万31个子行业第9名。各医药子行业中,医药流通(+1.49%)、医疗研发外包(+1.29%)、疫苗(+0.96%)表现居前,体外诊断(+0.06%)、其他生物制品(+0.35%)、医院(+0.40%)表现居后。个股方面,日涨幅榜前3位分别为泓博医药(+20.00%)、海特生物(+19.99%)、太极集团(+8.04%);跌幅榜前3位为济民医疗(-10.00%)、南华生物(-9.99%)、新天地(-9.68%)。行业要闻:5月14日,再生元宣布,美国FDA已接受其药品Dupixent(dupilumab)作为12至17岁青少年不充分控制的慢性鼻窦炎伴鼻息肉(CRSwNP)患者辅助维持治疗的补充生物制品许可申请(sBLA),并授予优先审评资格。FDA预计在2024年9月15日前完成审查,如果获批,Dupixent将成为美国FDA批准的首个针对12至17岁青少年不充分控制CRSwNP的治疗方案。(来源:再生元)公司要闻:国药现代(600420):公司发布公告,子公司国药集团容生制药有限公司收到国家药品监督管理局核准签发的帕拉米韦注射液《药品注册证书》,该药是新一代神经氨酸酶抑制剂,主要用于治疗甲型或乙型流感。通化东宝(600867):公司发布公告,近日收到国家药品监督管理局签发的关于德谷胰岛素利拉鲁肽注射液的药物临床试验批准通知书后,已经启动中国I期临床试验,并于近日成功完成首例患者给药。普利制药(300630):公司发布公告,近日收到国家药监局签发的马来酸曲美布汀片通过仿制药质量和疗效一致性评价的通知,该药是一种合成的抗胆碱能药物,主要用于治疗胃肠功能紊乱及肠易激综合征。佐力药业(300181):公司发布公告,近日收到国家药品监督管理局签发的灵香片《药物临床试验批准通知书》,同意该药开展用于盆腔炎性疾病后遗症慢性盆腔痛的临床试验。东亚药业(605177):公司发布公告,近日收到韩国食品药品监督管理局颁布的依帕司他原料药品注册证书,该药属于糖尿病用药,可抑制糖尿病病人体内山梨醇含量的异常升高,有效预防、改善和治疗糖尿病并发的末梢神经障碍,如麻木感、疼痛感等。风险提示:新药研发及上市不及预期;政策推进超预期;市场竞争加剧风险。
免责声明: 1.本站部分作品是由网友自主投稿和发布、编辑整理上传,对此类作品本站仅提供交流平台,不为其版权负责。 2.如发布机构认为违背了您的权益,请与我们联系,我们将对相关资料予以删除。 3.资源付费,仅为我们搜集整理和运营维护费用,感谢您的支持!
合集服务: 单个细分行业的合集获取请联系行研君:hanyanjun830
-
医药生物行业跟踪周报:IVD出海正当时,重点推荐新产业、迈瑞医疗等 东吴证券 2024-06-02(28页) 附下载

投资要点本周、年初至今医药指数涨幅分别为-0.94%、-13.6%,相对沪指的超额收益分别为-0.3...
1.53 MB共28页中文简体
4小时前61320积分
-
医药生物行业周报:自免BD风再起,新靶点新技术带来多项重磅交易 开源证券 2024-06-02(9页) 附下载

自免BD风再起,新靶点新技术带来多项重磅交易2024年,国内自免后期管线预计将陆续获批,商业化元年即...
1.19 MB共9页中文简体
4小时前48520积分
-
医药生物行业2024年5月投资策略:一季报整体表现承压,创新药商业化成效卓著 国信证券 2024-05-31(37页) 附下载

5月医药行业投资观点:创新动能和规范诊疗正在为行业积蓄反转力量。外部事件冲击,行业整顿事件持续影响,...
2.73 MB共37页中文简体
4小时前78520积分
-
电力设备及新能源行业新能源周报(第88期):重视光伏的“价极必反”,海外市场边际向好 太平洋 2024-05-31(32页) 附下载

报告摘要行业整体策略:重视光伏的“价极必反”,海外市场边际向好对于光伏产业链低价,海外市场逐步产生需...
1.89 MB共32页中文简体
4小时前85820积分
-
医药生物周报(24年第21周):ASCO摘要重点数据整理,2024年集采8号文解读 国信证券 2024-05-31(21页) 附下载
核心观点本周医药板块表现弱于市场,生物制品板块领跌。本周全部A股下跌2.20%(总市值加权平均),沪...
1.44 MB共21页中文简体
4小时前32820积分
-
医药生物行业专题研究:家用呼吸机:海外去库存有望迎来拐点 国联证券 2024-05-31(11页) 附下载

需求驱动家用呼吸机行业快速增长随着全球范围内呼吸慢病患者人数持续增加,相关医疗设备及耗材市场快速增长...
1.26 MB共11页中文简体
4小时前69120积分
-
道通科技 业绩重回高增长,充电桩业务势如破竹 太平洋 2024-05-31(5页) 附下载

道通科技(688208)2023&2024Q1业绩:2023年,公司实现营收实现营业收入32.51亿...
606.93 KB共5页中文简体
4小时前27918积分
-
6月金股 太平洋 2024-05-31(4页) 附下载

6月金股基本面逻辑:金融——瑞丰银行(601528.SH)公司非息收入支撑业绩发展,同时小微业务高增...
387.88 KB共4页中文简体
4小时前15410积分
-
医药生物行业2023年报及2024一季报分析之CRO、CDMO:寒冬已逝,黎明将临,底部区域积极配置 中泰证券 2024-05-30(15页) 附下载

投资要点2023年年报及2024年一季报CRO、CDMO板块完美收关,我们选取具有代表性、市场关注度...
854.36 KB共15页中文简体
3天前72220积分
-
医药行业周报:Insmed首创DPP1抑制剂NCFBE三期临床成功 太平洋 2024-05-30(3页) 附下载

报告摘要市场表现:2024年5月29日,医药板块涨跌幅-0.32%,跑输沪深300指数0.44pct...
539.54 KB共3页中文简体
3天前49520积分
-
恒瑞医药 再次成功转型,创新药已成为增长新引擎,静待启航 亿渡数据 2024-05-30(19页) 附下载

恒瑞医药(600276)主营业务:公司主要从事化学药物的研发、生产、销售业务,目前创新药占比接近5成...
1.13 MB共19页中文简体
3天前77318积分
-
比亚迪 第五代DM首搭秦L、海豹06,全球插混进入比亚迪时刻 太平洋 2024-05-30(5页) 附下载

比亚迪(002594)事件:5月28日,比亚迪第五代DM技术发布暨秦LDM-i、海豹06DM-i发布...
333.3 KB共5页中文简体
3天前8418积分
-
2024年康乃德生物医药企业研究报告 头豹研究院 2024-05-29(29页) 附下载

2024年康乃德生物医药企业研究报告本报告为康乃德生物医药企业研究报告, 基于公司2023年报发布热...
3.98 MB共29页中文简体
4天前69620积分
-
医药:罕见,集采还能提价?!国产长效干扰素绝对龙头:业绩节节攀升,又喜迎市场独占期 北京韬联科技 2024-05-29(16页) 附下载
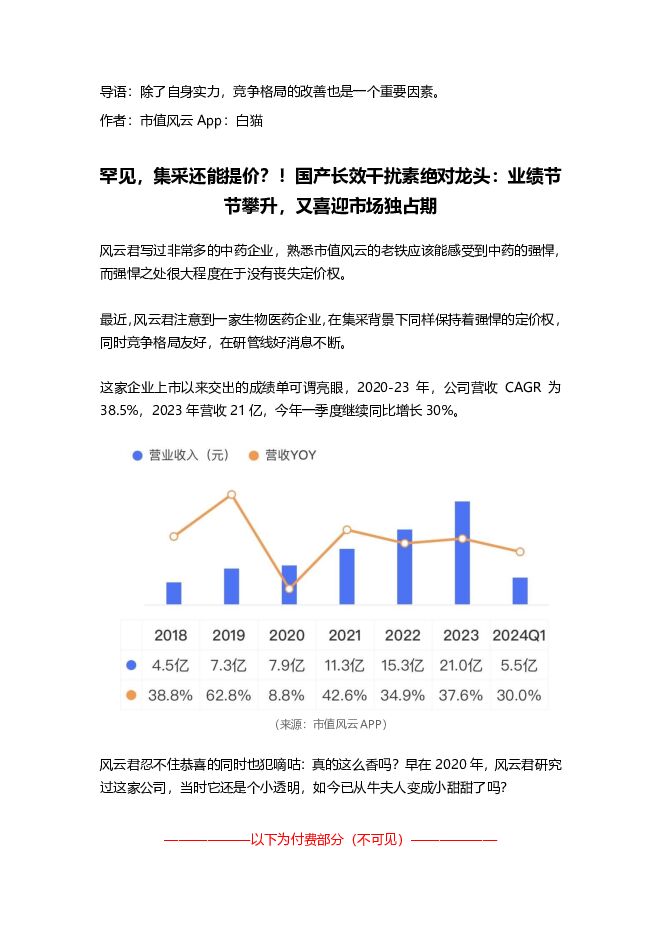
风云君写过非常多的中药企业,熟悉市值风云的老铁应该能感受到中药的强悍,而强悍之处很大程度在于没有丧失...
1.84 MB共16页中文简体
4天前63020积分
-
医药生物行业深度报告:分析借鉴国际药品定价经验,建立完善中国创新药价格体系 中国银河 2024-05-29(25页) 附下载

核心观点:借鉴海外药品定价模式:美国市场自由定价,日本类比参考定价,英国利润调控定价。①美国实行市场...
1.66 MB共25页中文简体
4天前40020积分
-
医药生物行业周报:人工关节接续采购落地,国产替代有望提速 甬兴证券 2024-05-29(8页) 附下载

行情回顾上周(2024年5月20日-5月24日),A股申万医药生物下跌3.74%,板块整体跑输沪深3...
864.72 KB共8页中文简体
4天前75220积分
-
医药与健康护理行业周报:《北京市加快医药健康协同创新行动计划(2024-2026年)》印发,支持创新药械发展 海通国际 2024-05-28(12页) 附下载

上周(0520-0524)上证综指下降2.1%,SW医药生物下降3.7%,涨跌幅在申万一级行业中排名...
2.08 MB共12页中文简体
5天前58020积分
-
医药生物行业双周报2024年第11期总第109期:《中国新药注册临床试验进展年度报告(2023年)》发布,2024年医药集中采购提质扩面 长城国瑞证券 2024-05-28(22页) 附下载

行业回顾本报告期医药生物行业指数跌幅为5.78%,在申万31个一级行业中位居第30,跑输沪深300指...
1.24 MB共22页中文简体
5天前18820积分
-
医药生物:纠风部际机制印发2024年医疗整顿指导性文件,严监管趋向常态化 中邮证券 2024-05-28(5页) 附下载
国家卫健委等14部委印发24年医疗整顿指导性文件事件:为切实做好2024年纠正医药购销领域和医疗服务...
667.81 KB共5页中文简体
5天前99320积分
-
汽车行业新势力周销量跟踪系列:理想领先,零跑亮眼 太平洋 2024-05-28(8页) 附下载

报告摘要新势力周销量跟踪:24年5月第2周(240506-240512)新势力品牌周销量数据来看,理...
560.54 KB共8页中文简体
5天前25420积分




